| Therapeutic area | Discovery | Preclinical | Phase I | Phase II | Phase III |
|---|---|---|---|---|---|
| NASH(AS-101) |  |
||||
| 염증성 장질환(AS-201) |  |
||||
| 황반변성(AS-301) |  |
||||
| 퇴행성 뇌질환(AS-401) |  |
- Home
- R&D
- Pipeline
Pipeline
- NASH
- 염증성 장질환
- 황반변성
- 퇴행성 뇌질환
NASH (Non-alcoholic Steatohepatitis, 비알코올성지방간염)
비알코올성 지방간염은 지방간(steatosis), 간염(inflammation), 간세포의 풍선화(ballooning) 소견을 보이며 병이 진전될 경우 간조직의 섬유화에 의해 간경화 및 간암으로 이어지는 심각한 질병입니다.
알코올 섭취와 무관하게 영양분을 과잉 섭취하는 서구화된 식습관이나 비만, 당뇨, 대사 증후군 등 여러 질환과 밀접하게 관련되어 있고 전 세계적으로 급속하게 증가하고 있어
2026년 약 30조원에 이르는 시장을 형성할 것으로 전문가들은 예측하고 있습니다.
그러나 발병 원인이 복잡하고 환자마다 다른 임상적인 양상을 보여 많은 치료제 개발 노력에도 불구하고 아직 승인된 치료제가 없는 상황입니다.
AS-101
AS-101은 새로운 타깃의 오토파지 작용제 (autophagy agonist)로써 경구투여가 가능한 비알코올성 지방간염 (NASH)치료제로 개발되고 있습니다.
AS-101은 간조직에서 선택적으로 높은 농도를 유지하면서 다양한 NASH 동물 모델에서 우수한 치료 효과를 보였음은 물론 독일과 일본에서 진행한 GLP 독성 시험을 통해 매우 안전한 치료제임을 확인하였습니다.
AS-101은 비알코올성 지방간염 치료제의 평가 지표인 NAFLD Activity Score (NAS, 비알코올성 지방간질환 활성지수)의 유의적인 감소와 간 조직에서 현저한 섬유화 면적의 감소를 확인하였습니다.
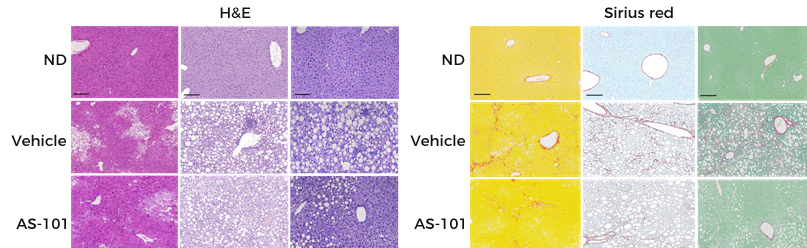
AS-101의 비임상 결과는 유럽 간학회(EASL 2020)에서 포스터로 발표되었고 우수 포스터로 선정되었습니다.
AS-101은 간세포(hepatocyte), 간 성상세포(hepatic stellate cell), 쿠퍼세포(Kupffer cell) 등 비알코올성 지방간염의 진행에 관련된 여러 세포에 총체적으로 작용해서
간조직의 기능 회복을 통해 치료 효과가 높을 것으로 기대됩니다.
또한 간조직에 선택적으로 작용하므로 전신 부작용 등의 독성이 적어 향후 비알코올성 지방간염의 1차 치료제 및 병용투여 치료제로 사용이 가능할 것입니다.
염증성 장질환 (IBD, inflammatory bowel disease) /
Leaky gut syndrome (장누수증후군)
장은 소화, 흡수, 배설 등의 기본적인 기능 이외에도 장의 점막이 미생물이나 이들의 부산물, 항원, 곰팡이 독소 등이 혈류로 유입되는 것을 차단하는 방어벽으로 작용하며 면역
데이터를 수집하는 역할을 동시에 수행하고 있습니다.
염증성 장질환은 재발과 호전을 반복하며 위장관에 염증을 일으키는 원인 불명의 만성질환으로 궤양성 대장염(Ulcerative colitis)과 크론병(Crohn's disease)이 대표적입니다.
염증성 장질환은 장에 생기는 심각한 만성 염증이 6개월 이상 지속되고, 오랜 기간 지속되는 만성적인 장관의 염증으로 인하여 장기적으로 삶의 질을 떨어뜨립니다. 합병증으로
장협착, 누공, 대장암의 발병 가능성이 높아지는 특징이 있으며 특히 치료제가 아직 없습니다.
장의 점막이 자극 등에 의해 손상되면 장점막 세포 사이의 결합이 약해지면서 틈이 발생하게 되는데 그때 세균, 곰팡이 등 여러 해로운 물질이 혈액 속에 유입되게 됩니다.
이렇게 되면 장내 염증이 발생이 발생하고 방어기능을 손상시키며 기존의 질환을 악화시킴과 동시에 천식, 아토피, 자폐증, 크론병 등 여러 다른 질환을 유발하게 되는데 이런
현상을 장누수증후군이라고 합니다.
AS-201
AS-201 은 장점막 세포에서 점액 생성 촉진 효과 및 관련 신호전달을 하는 단백질을 확인하였으며, 또한 장상피세포를 보호하고 융모 소실, 점막 궤양, 염증, 부종 등의 병변을 완화 및 감소시키는 효과를 확인하였습니다.
-
Indomethacin을 이용한 소장염 모델에서 AS-201의 효능확인
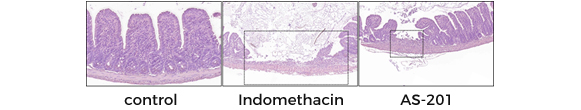
-
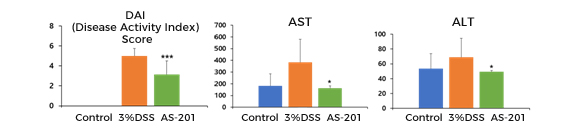
3% DSS 대장염 모델에서 AS-201의 효능확인
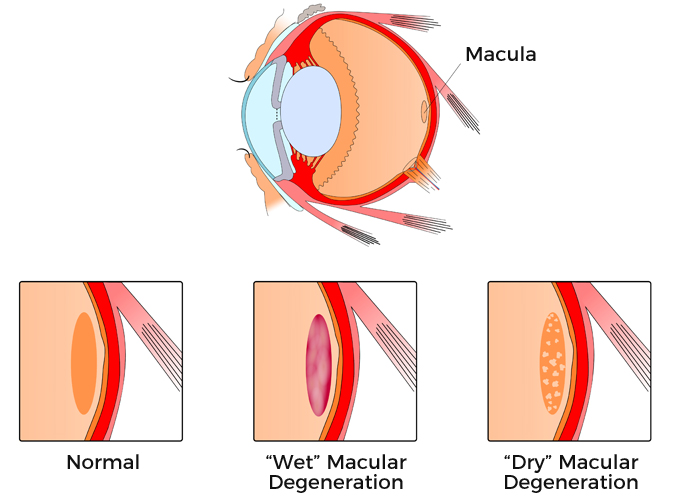
황반변성 (AMD, Age-related Macular Degeneration)
눈의 안쪽 망막의 중심부에 위치한 신경조직을 황반이라고 하는데, 시세포의 대부분이 이곳에 모여 있고 물체의 상이 맺히는 곳도 황반의 중심이므로 시력에 대단히 중요한 역할을 담당하고 있습니다.
이러한 황반이 노화, 유전적인 요인, 독성, 염증 등에 의해 기능이 떨어지면서 시력이 감소되고, 심할 경우 시력을 완전히 잃기도 하는 질환이 바로 연령관련 황반변성입니다.
황반변성의 원인은 명확하게 규명되지는 않았지만 노화에 따른 소수성의 노폐물 축적으로 인해 망막에 저산소증이 발생하여 황반부위의 신경세포가 서서히 퇴화하게 되는 것을 주요 원인으로 생각하고 있습니다.
이로 인해 망막과 맥락막에 비정상적인 혈관이 생기고, 이 혈관에서 누출된 혈액이나 액체가 원인이 되어 시력저하를 유발하는 것으로 보고 있습니다. 출혈의 위험이 있는
비정상적인 혈관을 생성시키는 원인으로는 나이 (연령), 흡연, 튀긴 음식, 햄버거 등의 고지방, 고열량 식습관, 스트레스, 비만, 고혈압, 혈중 콜레스테롤, 심혈관계 질환, 유전 및
가족력 등의 요소들이 영향을 미친다고 알려져 있습니다. 최근에는 스마트폰과 컴퓨터 모니터 등에 의해 노출되는 청색광 (Blue light)도 위험요인 중 하나로 알려져 있습니다.
AS-301
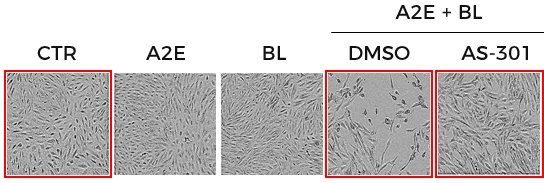
AS-301은 청색광에 노출된 인간 망막세포에 처리했을 때 대조군에 비해 망막색소상피세포의 보호 효과가 있음을 보여 오토파지 유도를 통한 치료제의 가능성이 확인되었고 보다 많은 연구를 통하여 황반변성 치료제의 개발을 진행하고 있습니다.
-
AMD모델 (A2E+Blue light)에서의 인간 망막세포 보호 효과
퇴행성 뇌질환 (Degenerative brain disease)
중뇌에 존재하는 도파민성 신경세포가 사멸하여 중추신경계에 주로 영향을 주는 질환으로 떨림, 경직성, 움직임이 늦거나 걷기가 어려운 등 비운동 증상뿐만이 아니라 치매,
우울증 등 정서적인 문제도 동반하여 알츠하이머, 파킨슨병 등 심각한 뇌질환을 유발하는 신경퇴행성 질환입니다.
도파민은 혈액뇌 장벽을 통과하지 못해 뇌에 부족한 도파민 수치를 높이는 약으로는 치료할 수 없기 때문에 현재 퇴행성 뇌질환을 개선시키는 치료제는 없으며 증상을 개선하는 대증요법을 사용하고 있습니다.
AS-401
오토파지사이언스가 개발하고 있는 퇴행성 뇌질환 치료 물질은 혈액뇌 장벽을 투과할 뿐만 아니라 뇌세포를 손상시키는 β-amyloid, synuclein, huntingtin 같은 단백질을
제거하기 위해 오토파지 현상을 활성화시키는 것을 확인하여 파킨슨뿐만 아니라 퇴행성 뇌질환 치료제의 개발 가능성을 높이 평가하고 있습니다.


